시험법
항생제 감수성 시험은 시험 균주의 오염, 부정확한 탁도 및 균주의 활성도 등에 따라 결과의 정확성이 떨어질 가능성이 있다. 따라서 매 시험마다 정확한 정도관리균주를 포함하여 시험하고, 정도관리 균주의 결과를 가장 먼저 확인한다. 정도관리 균주(51-53쪽 참조)의 결과가 허용 범위를 벗어난 경우는 해당 시험 결과를 신뢰할 수 없으므로 재실험을 시행한다.
감수성 시험 대상인 항생제는 다음의 원칙에 따라 선택하였다.
5-15-15 규칙 준수

| Antibiotics | SA | SE | SI | EF | EM | EC | KP | CI | EN | PA | AB | SL | SH | CA1 |
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Penicillin | D | D | D | D | ||||||||||
| Oxacillin | D | |||||||||||||
| Ampicillin | D | D | D | BD | BD | |||||||||
| Piperacillin | D | D | D | D | D | D | ||||||||
| Amoxicillin-clavulanic acid | D | D | D | D | ||||||||||
| Ampicillin-sulbactam | D | D | D | D | ||||||||||
| Piperacillin-Tazobactam | D | |||||||||||||
| Cefazolin | D | D | D | |||||||||||
| Cefotaxime | D | D | D | D | BD | BD | ||||||||
| Ceftriaxone | BD | BD | ||||||||||||
| Ceftazidime | D | D | D | D | D | D | BD | BD | ||||||
| Cefepime | D | D | D | D | D | D | ||||||||
| Cefoxitin | D | D | D | D | D | BD | BD | |||||||
| Aztreonam | D | D | D | D | ||||||||||
| Ertapenem | D | D | D | D | ||||||||||
| Imipenem | D, AD | D, AD | D, AD | D, AD | D | D | BD | BD | ||||||
| Meropenem | D, AD | D, AD | D, AD | D, AD | D | D | ||||||||
| Erythromycin | D | D | D | D | ||||||||||
| Azithromycin | BD | BD | ||||||||||||
| Clindamycin | D | D | D | |||||||||||
| Quinupristin-dalfopristin | D | D | D | D | ||||||||||
| Amikacin | D | D | D | D | D | D | BD | BD | ||||||
| Gentamicin | D | D | D | D | D | D | D | D | D | BD | BD | |||
| Streptomycin | BD | BD | ||||||||||||
| Tobramycin | D | D | D | D | D | D | ||||||||
| Gentamicin-High Level | D | D | ||||||||||||
| Streptomycin-High Level | D | D | ||||||||||||
| Ciprofloxacin | D | D | D | D | D | D | D | D | BD | BD | D | |||
| Nalidixic acid | D | D | D | D | BD | BD | ||||||||
| Tetracycline | D | D | D | D | D | D | D | D | D | D | BD | BD | D | |
| Minocycline | D | |||||||||||||
| Tigecycline | E | E | E | E | E | D | D | D | D | D | ||||
| Vancomycin | E | E | E | E | E | |||||||||
| Teicoplanin | E | E | E | E | E | |||||||||
| Trimethoprime- sulfamethoxazole | D | D | D | D | D | D | D | BD | BD | |||||
| Mupirocin | D | D | D | |||||||||||
| Linezolid | E | E | E | E | E | |||||||||
| Chloramphenicol | D | D | D | D | D | D | D | D | D | BD | BD | |||
| Nitrofurantoin | D | D | D | D | D | D | ||||||||
| Rifampicin | D | D | D | |||||||||||
| Colistin | BD | BD | BD | BD | BD | BD | BD | BD |
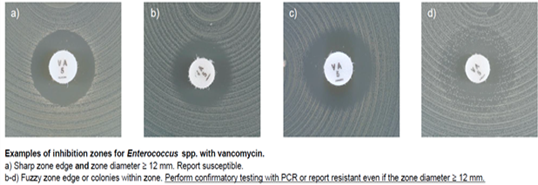
균종별로 적용 가능한 판독 기준은 미국의 Clinical and Laboratory Standards Institute (CLSI) M100-S27 Peformance standards for antimicrobial susceptibility testing (2017)을 적용하였고, 판독 기준이 없는 일부 항균제는 유럽의 The European Committee on Antimicrobial Susceptibility Testing. Breakpoint tables for interpretation of MICs and zone diameters. Version 7.1, (2017)을 적용하였다 (EUCAST 표시). S. epidermidis 및 S. pseudintermedius의 mupirocin 판독기준은 EUCAST의 S. aureus 기준을 적용하였다.
| 균종 | 항생제 | 용량(µg) | 판독기준(mm) | ||
|---|---|---|---|---|---|
| ≥S | I | ≤R | |||
| S. aureus | Penicillin | 10U | 29 | 28 | |
| Cefoxitin | 30 | 22 | 21 | ||
| Erythromycin | 15 | 23 | 14-22 | 13 | |
| Clindamycin | 2 | 21 | 15-20 | 14 | |
| Trimethoprim-sulfamethoxazole | 1.25/23.75 | 16 | 11-15 | 10 | |
| Quinuprisitn-dalfopristin | 15 | 19 | 16-18 | 15 | |
| Tetracycline | 30 | 19 | 15-18 | 14 | |
| Mupirocin (EUCAST) | 200 | 30 | 18-29 | 17 | |
| Cholramphenicol | 30 | 18 | 13-17 | 12 | |
| Rifampicin | 5 | 20 | 17-19 | 16 | |
| S. epidermidis | Penicillin | 10U | 29 | 28 | |
| Cefoxitin | 1 | 25 | 24 | ||
| Erythromycin | 15 | 23 | 14-22 | 13 | |
| Clindamycin | 2 | 21 | 15-20 | 14 | |
| Trimethoprim-sulfamethoxazole | 1.25/23.75 | 16 | 11-15 | 10 | |
| Quinuprisitn-dalfopristin | 15 | 19 | 16-18 | 15 | |
| Tetracycline | 30 | 19 | 15-18 | 14 | |
| Mupirocin (EUCAST) | 200 | 30 | 18-29 | 17 | |
| Cholramphenicol | 30 | 18 | 13-17 | 12 | |
| Rifampicin | 5 | 20 | 17-19 | 16 | |
| S. pseudintermedius | Penicillin | 10U | 29 | 28 | |
| Oxacillin | 30 | 18 | 17 | ||
| Erythromycin | 15 | 23 | 14-22 | 13 | |
| Clindamycin | 2 | 21 | 15-20 | 14 | |
| Trimethoprim-sulfamethoxazole | 1.25/23.75 | 16 | 11-15 | 10 | |
| Quinuprisitn-dalfopristin | 15 | 19 | 16-18 | 15 | |
| Tetracycline | 30 | 19 | 15-18 | 14 | |
| Mupirocin (EUCAST) | 200 | 30 | 18-29 | 17 | |
| Cholramphenicol | 30 | 18 | 13-17 | 12 | |
| Rifampicin | 5 | 20 | 17-19 | 16 | |
| E. faecium | Penicillin | 10U | 15 | 14 | |
| Ampicillin | 10 | 17 | 16 | ||
| Gentamicin (High level) | 120 | 10 | 7-9 | 6 | |
| Streptomycin (High level) | 300 | 10 | 7-9 | 6 | |
| Ciprofloxacin | 5 | 21 | 16-20 | 15 | |
| Tetracycline | 30 | 19 | 15-18 | 14 | |
| Cholramphenicol | 30 | 18 | 13-17 | 12 | |
| Nitrofurantoin | 300 | 17 | 15-16 | 14 | |
| E. faecalis | Ampicillin | 10 | 17 | 16 | |
| Gentamicin (High level) | 120 | 10 | 7-9 | 6 | |
| Streptomycin (High level) | 300 | 10 | 7-9 | 6 | |
| Ciprofloxacin | 5 | 21 | 16-20 | 15 | |
| Tetracycline | 30 | 19 | 15-18 | 14 | |
| Quinuprisitn-dalfopristin | 15 | 19 | 16-18 | 15 | |
| Cholramphenicol | 30 | 18 | 13-17 | 12 | |
| Nitrofurantoin | 300 | 17 | 15-16 | 14 | |
| E. coli | Ampicillin | 10 | 17 | 14-16 | 13 |
| Piperacillin | 100 | 21 | 18-20 | 17 | |
| Ampicillin-sulbactam | 10/10 | 15 | 12-14 | 11 | |
| Amoxillin-clavulanate | 20/10 | 18 | 14-17 | 13 | |
| Cefazolin | 30 | 23 | 20-22 | 19 | |
| Cefotaxime | 30 | 26 | 23-25 | 22 | |
| Ceftazidime | 30 | 21 | 18-20 | 17 | |
| Cefepime | 30 | 25 | 19-24 | 18 | |
| Aztreonam | 30 | 21 | 18-20 | 17 | |
| Cefoxitin | 30 | 18 | 15-17 | 14 | |
| Imipenem | 10 | 23 | 20-22 | 19 | |
| Meropenem | 10 | 23 | 20-22 | 19 | |
| Ertapenem | 10 | 22 | 19-21 | 18 | |
| Amikacin | 30 | 17 | 15-16 | 14 | |
| Gentamicin | 10 | 15 | 13-14 | 12 | |
| Ciprofloxacin | 5 | 21 | 16-20 | 15 | |
| Naldixic acdi | 30 | 19 | 14-18 | 13 | |
| Trimethoprim-sulfamethoxazole | 1.25/23.75 | 16 | 11-15 | 10 | |
| Tetracycline | 30 | 15 | 12-14 | 11 | |
| Tigecycline (EUCAST) | 15 | 18 | 17-15 | 14 | |
| Chloramphenicol | 30 | 18 | 13-17 | 12 | |
| Nitrofurantoin | 300 | 17 | 15-16 | 14 | |
| K. pneumoniae | Piperacillin | 100 | 21 | 18-20 | 17 |
| Ampicillin-sulbactam | 10/10 | 15 | 12-14 | 11 | |
| Amoxillin-clavulanate | 20/10 | 18 | 14-17 | 13 | |
| Cefazolin | 30 | 23 | 20-22 | 19 | |
| Cefotaxime | 30 | 26 | 23-25 | 22 | |
| Ceftazidime | 30 | 21 | 18-20 | 17 | |
| Cefepime | 30 | 25 | 19-24 | 18 | |
| Aztreonam | 30 | 21 | 18-20 | 17 | |
| Cefoxitin | 30 | 18 | 15-17 | 14 | |
| Imipenem | 10 | 23 | 20-22 | 19 | |
| Meropenem | 10 | 23 | 20-22 | 19 | |
| Ertapenem | 10 | 22 | 19-21 | 18 | |
| Amikacin | 30 | 17 | 15-16 | 14 | |
| Gentamicin | 10 | 15 | 13-14 | 12 | |
| Ciprofloxacin | 5 | 21 | 16-20 | 15 | |
| Naldixic acdi | 30 | 19 | 14-18 | 13 | |
| Trimethoprim-sulfamethoxazole | 1.25/23.75 | 16 | 11-15 | 10 | |
| Tetracycline | 30 | 15 | 12-14 | 11 | |
| Tigecycline (EUCAST) | 15 | 18 | 17-15 | 14 | |
| Chloramphenicol | 30 | 18 | 13-17 | 12 | |
| Nitrofurantoin | 300 | 17 | 15-16 | 14 | |
| Citrobacter spp. | Piperacillin | 100 | 21 | 18-20 | 17 |
| Ampicillin-sulbactam(C. freundii 자연내성) | 10/10 | 15 | 12-14 | 11 | |
| Amoxillin-clavulanate | 20/10 | 18 | 14-17 | 13 | |
| Cefazolin | 30 | 23 | 20-22 | 19 | |
| Cefotaxime | 30 | 26 | 23-25 | 22 | |
| Ceftazidime | 30 | 21 | 18-20 | 17 | |
| Cefepime | 30 | 25 | 19-24 | 18 | |
| Aztreonam | 30 | 21 | 18-20 | 17 | |
| Cefoxitin | 30 | 18 | 15-17 | 14 | |
| Imipenem | 10 | 23 | 20-22 | 19 | |
| Meropenem | 10 | 23 | 20-22 | 19 | |
| Ertapenem | 10 | 22 | 19-21 | 18 | |
| Amikacin | 30 | 17 | 15-16 | 14 | |
| Gentamicin | 10 | 15 | 13-14 | 12 | |
| Ciprofloxacin | 5 | 21 | 16-20 | 15 | |
| Naldixic acdi | 30 | 19 | 14-18 | 13 | |
| Trimethoprim-sulfamethoxazole | 1.25/23.75 | 16 | 11-15 | 10 | |
| Tetracycline | 30 | 15 | 12-14 | 11 | |
| Tigecycline (EUCAST) | 15 | 18 | 17-15 | 14 | |
| Chloramphenicol | 30 | 18 | 13-17 | 12 | |
| Nitrofurantoin | 300 | 17 | 15-16 | 14 | |
| Enterobacter spp. | Piperacillin | 100 | 21 | 18-20 | 17 |
| Amoxillin-clavulanate | 20/10 | 18 | 14-17 | 13 | |
| Cefotaxime | 30 | 26 | 23-25 | 22 | |
| Ceftazidime | 30 | 21 | 18-20 | 17 | |
| Cefepime | 30 | 25 | 19-24 | 18 | |
| Aztreonam | 30 | 21 | 18-20 | 17 | |
| Imipenem | 10 | 23 | 20-22 | 19 | |
| Meropenem | 10 | 23 | 20-22 | 19 | |
| Ertapenem | 10 | 22 | 19-21 | 18 | |
| Amikacin | 30 | 17 | 15-16 | 14 | |
| Gentamicin | 10 | 15 | 13-14 | 12 | |
| Ciprofloxacin | 5 | 21 | 16-20 | 15 | |
| Naldixic acdi | 30 | 19 | 14-18 | 13 | |
| Trimethoprim-sulfamethoxazole | 1.25/23.75 | 16 | 11-15 | 10 | |
| Tetracycline | 30 | 15 | 12-14 | 11 | |
| Tigecycline (EUCAST) | 15 | 18 | 17-15 | 14 | |
| Chloramphenicol | 30 | 18 | 13-17 | 12 | |
| Nitrofurantoin | 300 | 17 | 15-16 | 14 | |
| P. aeruginosa | Piperacillin | 100 | 21 | 15-20 | 14 |
| Piperacillin-tazobactam | 100/10 | 21 | 15-20 | 14 | |
| Ceftazidime | 30 | 18 | 15-17 | 14 | |
| Cefepime | 30 | 18 | 15-17 | 14 | |
| Imipenem | 10 | 19 | 16-18 | 15 | |
| Meropenem | 10 | 19 | 16-18 | 15 | |
| Amikacin | 30 | 17 | 15-16 | 14 | |
| Gentamicin | 10 | 15 | 13-14 | 12 | |
| Tobramycin | 10 | 15 | 13-14 | 12 | |
| Ciprofloxacin | 5 | 21 | 16-20 | 15 | |
| Acinetobacter spp. | Piperacillin | 100 | 21 | 18-20 | 17 |
| Ampicillin-sulbactam | 10/10 | 15 | 12-14 | 11 | |
| Ceftazidime | 30 | 18 | 15-17 | 14 | |
| Cefepime | 30 | 18 | 15-17 | 14 | |
| Imipenem | 10 | 22 | 19-21 | 18 | |
| Meropenem | 10 | 18 | 15-17 | 14 | |
| Amikacin | 30 | 17 | 15-16 | 14 | |
| Gentamicin | 10 | 15 | 13-14 | 12 | |
| Tobramycin | 10 | 15 | 13-14 | 12 | |
| Ciprofloxacin | 5 | 21 | 16-20 | 15 | |
| Tetracycline | 30 | 15 | 12-14 | 11 | |
| Minocycline | 30 | 16 | 13-15 | 12 | |
| Tigecycline (EUCAST) | 15 | 18 | 17-15 | 14 | |
| Campylobacterspp. | Erythromycin | 15 | 16 | 13-15 | 12 |
| Ciprofloxacin | 5 | 24 | 21-23 | 20 | |
| Tetracycline | 30 | 26 | 23-25 | 22 | |
시험 항생제의 숫자에 따라 Mueller-Hinton 한천배지 90mm와 150mm 크기를 사용한다. 배지의 두께는 중심부부터 가장 자리까지 4mm로 일정하게 유지되어야 한다.
면봉에 균액을 묻히고 과량의 액체는 면봉을 시험관 벽에 대고 돌리어 짜낸 후에 접종한다 (균액을 만들고 15분 이내에 접종). 균액은 배지를 120°씩 돌려서 3번을 바르도록 한다.
균액을 접종하고 3-5분 후에 물기가 마르면 스트립을 놓고, 떨어진 스트립은 이동을 금지한다(균액 접종 후 15분 이내에 스트립 접종).



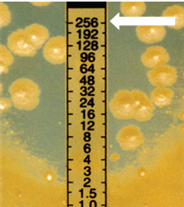

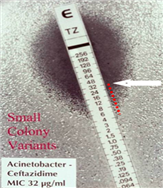


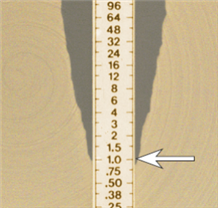
| 균종 | 항생제 | 판독기준(µg/mL) | ||
|---|---|---|---|---|
| ≥S | I | ≤R | ||
| S. aureus | Vancomycin | 2 | 4-8 | 16 |
| Teicoplanin | 8 | 16 | 32 | |
| Linezolid | 4 | NA | 8 | |
| Tigecycline (EUCAST, BMD) | 0.5 | NA | 1 | |
| S. epidermidisS. pseudintermedius | Vancomycin | 4 | 8-16 | 32 |
| Teicoplanin | 8 | 16 | 32 | |
| Linezolid | 4 | NA | 8 | |
| Tigecycline (EUCAST, BMD) | 0.5 | NA | 1 | |
| E. faeciumE. faecalis | Vancomycin (24hr incubation) | 4 | 8-16 | 32 |
| Teicoplanin | 8 | 16 | 32 | |
| Linezolid | 2 | 4 | 8 | |
| Tigecycline (EUCAST, BMD) | 0.25 | 0.5 | 1 | |

| 균종 | 항생제 | 판독기준(µg/mL) | ||
|---|---|---|---|---|
| ≥S | I | ≤R | ||
| Salmonellaspp. | Ampicillin | 8 | 16 | 32 |
| Cefotaxime | 1 | 2 | 4 | |
| Ceftriaxone | 1 | 2 | 4 | |
| Ceftazidime | 4 | 8 | 16 | |
| Cefoxitin | 8 | 16 | 32 | |
| Imipenem | 1 | 2 | 4 | |
| Ciprofloxacin | 0.06 | 0.12-0.5 | 1 | |
| Nalidixic acid (EUCAST) | NA | NA | NA | |
| Amikacin | 16 | 32 | 64 | |
| Gentamicin | 4 | 8 | 16 | |
| Streptomycin | NA | NA | NA | |
| Tetracycline | 4 | 8 | 16 | |
| Trimethoprim-Sulfamethoxazole | 2/38 | NA | 4/76 | |
| Azithromycin (S. Typhi only) | 16 | NA | 32 | |
| Colistin | 2 | NA | 4 | |
| Shigellaspp. | Ampicillin | 8 | 16 | 32 |
| Cefotaxime | 1 | 2 | 4 | |
| Ceftriaxone | 1 | 2 | 4 | |
| Ceftazidime | 4 | 8 | 16 | |
| Cefoxitin | 8 | 16 | 32 | |
| Imipenem | 1 | 2 | 4 | |
| Ciprofloxacin | 1 | 2 | 4 | |
| Nalidixic acid | 16 | NA | 32 | |
| Amikacin | 16 | 32 | 64 | |
| Gentamicin | 4 | 8 | 16 | |
| Streptomycin | NA | NA | NA | |
| Tetracycline | 4 | 8 | 16 | |
| Trimethoprim-Sulfamethoxazole | 2/38 | NA | 4/76 | |
| Azithromycin (S. flexneri, ECOFF) | 8 | NA | 16 | |
| Azithromycin (S. sonnei, ECOFF) | 16 | NA | 32 | |
| Colistin | 2 | NA | 4 | |